Das angeborene Immunsystem zeichnet sich dadurch aus, dass Immun-Zellen und sogenannte humorale Bestandteile von Geburt an, also schon im Babykörper vorhanden und gewappnet sind direkt in Aktion zu treten.
Zu den angeborenen und humoralen Bestandteilen des Immunsystems zählen zum Beispiel physiologische Barrieren wie die Haut, Schleimhäute in Mund, Nase und Atemwege aber auch Magen und Darmtrakt. Ein weiterer Bestandteil in dem Bereich sind BotenstoffeZytokine sind Signalstoffe die von Zellen sekretiert (abgege... More und das KomplementsystemDas Komplementsystem besteht aus zahlreichen Bestandteilen u... More.
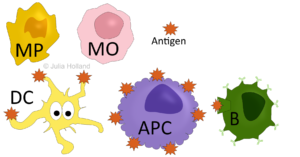
Es gibt aber darüber hinaus auch noch die Immun-Zellen (Zellulären Bestandteile). Aufzuzählen wären da unter anderem die
- MakrophagenDie Hauptaufgabe der Makrophagen ist Erkennung der Fremdkör... More,
- Granulozyten Granulozyten gehören zu den weißen Blutkörperchen ... More,
- Neutrophilen Granulozyten gehören zu den weißen Blutkörperchen ... More,
- NKNatürliche-Killer-Zellen (NK-Zellen) sind weiße Blutkörpe... More (Natürlichen Killer) Zellen,
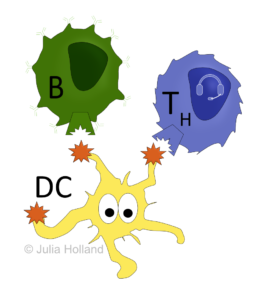
- DCsDendritische Zellen sind als Antigen-präsentierende-Zellen ... More (englisch: Dendritic cells = Dendritische ZellenDendritische Zellen sind als Antigen-präsentierende-Zellen ... More).
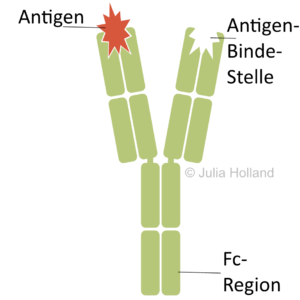
Alle genannten Komponenten zusammen stellen die erste Verteidigungslinie des Immunsystems dar. Es gibt zusätzlich im Körper – und das ist sehr wichtig –auch ein Erkennungssystem, um FremdkörperSind Dinge, Lebewesen, oder Moleküle, die nicht natürlich ... More von körpereigenen Zellen zu unterscheiden. Der wichtigste Baustein dieses Systems heißt AntigenJede Zelle eines Menschen hat Erkennungsmerkmale auf seiner ... More.